Johnson&Johnson pide la autorización para su vacuna en Estados Unidos
Este antídoto, a diferencia de las vacunas de Pfizer y BioNTech y Moderna, no requiere una segunda inyección ni una cadena de frío para su transporte y conservación.
5 feb 2021 - 09:35
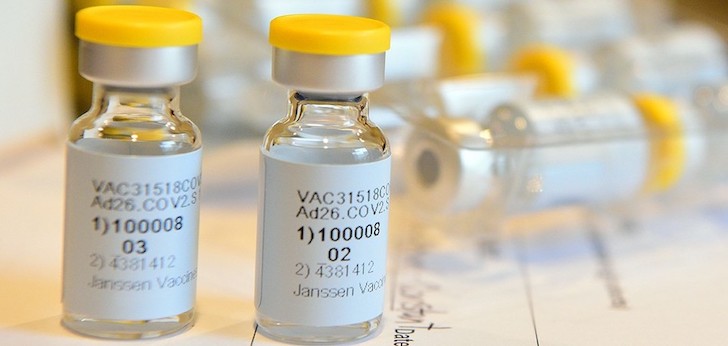
Johnson&Johnson, más cerca de comercializar su vacuna. La farmacéutica estadounidense ha solicitado la autorización para su vacuna contra el Covid-19 en Estados Unidos. La Agencia Estadounidense del Medicamento (FDA, por sus siglas en inglés) deberá convocar una reunión de su panel de expertos en vacunas para revisar los datos presentados por el grupo y emitir una recomendación.
La vacuna de Johnson&Johnson se caracteriza porque no requiere una segunda inyección ni una cadena de frío para su transporte y conservación, a diferencia de las otras dos vacunas actualmente autorizadas en Estados Unidos, que son las de Pfizer y BioNTech y la de Moderna.
La aprobación de esta nueva vacuna supondría un importante impulso en el proceso de vacunación de Estados Unidos, especialmente porque se administra con una única dosis. Johnson&Johnson indica en un comunicado que espera que el producto esté listo para su distribución “inmediatamente después de la autorización”.
Johnson&Johnson prevé cumplir con su compromiso de entregar cien millones de dosis para mediados de 2021
El grupo estima cumplir con su compromiso de entregar cien millones de dosis para mediados de 2021. “Estamos trabajando con gran urgencia para que nuestra vacuna en investigación esté disponible al público lo antes posible”, ha explicado el vicepresidente del comité ejecutivo y científico de Johnson&Johnson, Paul Stoffels.
Los datos del ensayo clínico de la farmacéutica muestran que su vacuna tiene una eficacia del 66%. Los resultados en un estudio en el que participaron casi 44.000 voluntarios registró una eficacia del 72% en Estados Unidos, un 66% en Latinoamérica y un 57% en Sudáfrica.